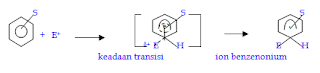
Mekanisme Reaksi Substitusi
Nukleofilik
Reaksi yang berlangsung karena penggantian
satu atau lebih atom atau gugus dari suatu senyawa oleh atom atau gugus lain
disebut reaksi substitusi. Bila reaksi substitusi melibatkan nukleofil, maka
reaksi disebut substitusi nukleofilik (SN), dimana S menyatakan
substitusi dan N menyatakan nukleofilik.
Spesies
yang bertindak sebagai penyerang adalah nukleofil
(basa Lewis), yaitu spesies yang dapat memberikan pasangan elektron ke atom
lain untuk membentuk ikatan kovalen. Perubahan yang terjadi pada reaksi ini
pada dasarnya adalah suatu nukleofil dengan membawa pasangan elektronnya
menyerang substrat (molekul yang menyediakan karbon untuk pembentukan ikatan
baru), membentuk ikatan baru dan salah satu substituen pada atom karbon lepas
bersama berpasangan elektronnya.
Jika
nukleofil penyerang dinyatakan dengan lambang Y: atau Y dan substratnya R-X;
maka persaman reaksi substitusi nukleofilik dapat dituliskan secara sederhana
sebagai berikut:
Substrat nukleofil hasil
substitusi gugus pergi
Gugus
pergi adalah substituen yang lepas dari substrat, yang berarti atom atau
gugus apa saja yang digeser dari ikatannya dengan atom karbon. Substrat bisa bermuatan
netral atau positif, sedangkan nukleofil bermuatan netral atau negatif. Pada
umumnya nukleofil adalah ion yang bermuatan negatif (anion), tetapi beberapa
molekul netral dapat pula bertindak sebagai nukleofil, contoh: H2O,
CH3OH, dan CH3NH2. Hal ini disebabkan karena
molekul-molekul netral tersebut, memiliki pasangan elektron menyendiri yang
dapat digunakan untuk membentuk ikatan sigma dengan atom C substrat. Dalam
reaksi substitusi nukleofilik bila nukleofilnya H2O atau -OH disebut
reaksi hidrolisis, sedangkan bila
nukleofil penyerangnya berupa pelarut disebut reaksi solvolisis. Dengan demikian maka reaksi substitusi
nukleofilik dapat dituliskan dalam 4
macam persamaan reaksi, yaitu :
Nu: – +
R – L → Nu
– R + L: –
Nu:
+
R – L → Nu+ – R
+ L: –
Nu: – +
R – L+ →
Nu – R + L:
Nu: – +
R – L+ →
Nu+ – R + L:
Keterangan
:
Nu : atau Nu:¯ adalah nukleofil
L : atau L:¯ adalah gugus pergi
Gugus pergi dan
pengaruh gugus tetangga
Gugus pergi adalah gugus yang mudah putus apabila terjadi reaksi
substitusi , dan kemudian di gantikan oleh gugus dari senyawa lain ( gugus
tetangga). Reaksi-reaksi senyawa karbon reaksi senyawa karbon dapat
dapat terjadi dengan berbagai cara, seperti reaksi substitusi, reaksi adisi dan
reaksi eliminasi. Reaksi substitusi reaksi substitusi atau disebut reaksi
pertukaran gugus fungsi terjadi saat atom atau gugus atom dari suatu senyawa
karbon digantikan oleh atom atau gugus atom lain dari senyawa yang lain.
Reaksi
substitusi
Reaksi substitusi atau disebut reaksi pertukaran gugus fungsi terjadi saat
atom atau gugus atom dari suatu senyawa karbon digantikan oleh atom atau gugus
atom lain dari senyawa yang lain. Secara umum mekanismenya :
Atom karbon ujung suatu alkil halida mempunyai muatan positif parsial.
Karbon ini bisa rentan terhadap (susceptible; mudah diserang oleh) serangan
oleh anion dan spesi lain apa saja yang mempunyai sepasang elektron menyendiri
(unshared) dalam kulit luarnya. Dihasilkan reaksi subtitusi –suatu reaksi dalam
mana satu atom, ion atau gugus disubstitusikan untuk (menggantikan) atom, atau
gugus lain.
Dalam suatu reaksi substitusi alkil halida, halida itu disebut gugus pergi
(leaving group) suatu istilah yang berarti gugus apa saja yang dapat
digeser dari ikatannya dengan suatu atom karbon. Ion Halida merupakan gugus pergi
yang baik, karena ion-ion ini merupakan basa yang sangat lemah. Basa kuat
seperti misalnya OH-, bukan gugus pergi yang baik.
Spesi (spesies) yang menyerang suatu alkil halida dalam suatu reaksi
substitusi disebut nukleofil (nucleophile, “pecinta nukleus”), sering
dilambangkan dengan Nu-. Dalam persamaan reaksi diatas, OH- dan CH3O-,
adalah nukleofil. Umumnya, sebuah nukleofil ialah spesi apa saja yang tertarik
ke suatu pusat positif ; jadi sebuah nukleofil adalah suatu basa Lewis.
Kebanyakan nukleofil adalah anion, namun beberapa molekul polar yang netral,
seperti H2O, CH3OH dan CH3NH2 dapat
juga bertindak sebagai nukleofil. Molekul netral ini memiliki pasangan elektron
menyendiri, yang dapat digunakan untuk membentuk ikatan sigma. Nukleofil ialah
elektrofil (“pecinta elektron”) sering dilambangkan dengan E+. Suatu elektrofil
ialah spesi apa saja yang tertarik ke suatu pusat negatif, jadi suatu
elektrofil ialah suatu asam Lewis seperti H+ atau ZnCl2. Beberapa
reaksi substitusi :
a. Reaksi alkila halida dengan basa kuat
b. Reaksi alkohol dengan PCl3
c. Reaksi alkohol dengan logam Natrium
d. Reaksi klorinasi
e. Reaksi esterifikasi (pembentukan ester)
f. Reaksi saponifikasi (penyabunan)
Reaksi Adisi
Reaksi adisi terjadi jika senyawa karbon yang mempunyai ikatan rangkap
menerima atom atau gugus atom lain sehingga ikatan rangkap berubah menjadi
ikatan tunggal. Ikatan rangkap merupakan ikatan tak jenuh, sedangkan ikatan
tunggal merupakan ikatan jenuh. Jadi, reaksi adisi terjadi dari ikatan tak
jenuh menjadi ikatan jenuh.
Mekanismenya
reaksi adisi :
C = C → C- C
C ≡ C → C = C → C – C
Beberapa reaksi
adisi :
a. Reaksi hidrogenasi alkana
R – CH = CH – R’ + H – H → R – CH2 – CH2 – R’
Contoh :
C2H5 – CH = CH – CH3 + H – H →
C2H5 – CH – CH – CH3
2-pentena
n-pentana
Reaksi
hidrogenasi ini digunakan untuk membuat margarin (mentega tiruan) dari minyak
yang mengandung asam lemak tak jenuh (C = C). Minyak cair dihidrogenasi dengan
bantuan katalis Ni menghasilkan lemak padat.
b. Reaksi adisi dengan halogen
Reaksi adisi dengan brom digunakan untuk membedakan senyawa alkena (C = C)
dengan sikloalkana. Hal ini karena kedua senyawa mempunyai isomer fungsional
(rumus molekul sama, tetapi gugus fungsi berbeda). Pengamatan reaksinya dengan
membedakan warna dari brom yaitu merah coklat. Alkena dapat bereaksi dengan
brom sehingga warna merah coklat dari brom hilang menjadi tidak berwarna. Akan
tetapi, sikloalkana tidak bereaksi dan warna merah coklat dari brom tetap.
Alkena + brom → bereaksi,
warna merah coklat dari brom hilang
Sikloalkana + brom tidak
bereaksi, warna merah coklat dari brom tetap.
c. Adisi dengan asam halida (HX)
R – CH = CH – R’ + H – X → R – CH – CH – R’
|
|
H X
Dalam adisi ini
atom X terikat pada C rangkap dikiri atau dikanan akan menghasilkan senyawa
yang berbeda, kecuali kalau R dengan R’ sama. Untuk itu, ada aturan yang
(padat) menetapkan hasil utama dari reaksi adisi tersebut yang dikemukakan oleh
Vlademir Markovnikov.
Reaksi
eliminasi
Reaksi Eliminasi adalah reaksi penghilangan suatu gugus atom pada suatu
senyawa. Pada reaksi elimiasi teradi perubahan ikatan, ikatan tunggal –>
ikatan rangkap.
Contoh :
CH3–CH3 –>
CH2=CH2 + H2
CH3–CH2Br
–> CH2=CH2 + HBr
CH3–CH2OH
–> CH2=CH2 + H2O
Partisipasi
Gugus Tetangga
partisipasi gugus tetangga didefinisikan sebagai gugus yang memberikan
suatu reaksi intermediate yang baru pada pusat reaksi. Untuk reaksi substitusi
seperti dibawah, X sebagai gugus tetangga berperan dalam penyerangan nukleofilik
intramolekul sehingga melepaskan Y sebagai gugus pergi, yang kemudian diikuti
oleh substitusi intermolekul.
Hasil dari partisipasi ini ialah pembentukan produk substitusi dengan
konfigurasi yang berlawanan dengan konfigurasi yang seharusnya terjadi pada
SN2, dimana reaksi SN2 pada umumnya membentuk konfigurasi yang berlawanan
dengan substrat. Dengan adanya partisipasi gugus tetangga, konfigurasi produk
sama dengan substrat. Partisipasi gugus tetangga ini juga dapat mempengaruhi
kecepatan reaksi.
Partisipasi Nitrogen
Sebagai Gugus Tetangga
Partisipasi
nitrogen sebagai gugus tetangga dapat terjadi dalam bentuk aminanya, seperti
reaksi substitusi senyawa amina di bawah ini :
kinetika reaksi diatas merupakan reaksi orde satu. Kecepatan reaksi
tergantung hanya pada konsentrasi substrat tapi tidak pada nukleofiliknya. Hal
ini mengherankan, dimana substitusi nukleofilik atom karbon primer SN2
kecepatan reaksinya tergantung pada konsentrasi substrat dan nukleofilik.
Tetapi dengan adanya partisipasi gugus tetangga mengakibatkan kecepatan
reaksinya hanya bergantung kepada konsentrasi substratnya saja.
Pertanyaan
:
1. Ion atau molekul apa saja gugus pergi yang
baik digunakan dan tidak baik yang digunakan? Jelaskan!
2. Apa saja aturan markovnikov
tersebut dalam reaksi adisi dengan asam halida? Jelaskan!
3. Apa ynag dapat mempengaruhi partisipasi gugus
tetangga tersebut? Jelaskan!
4. Apakah ada partisipasi lainnya selain nitrogen
sebagai gugus tetangga? Jelaskan!
Sumber : Fessenden, R. J. Dan J. S. Fessenden. 1982. Kimia organic edisi ketiga. Jakarta : Erlangga.
Hart, H. 1987. Kimia
Organik. Jakatra : Erlangga.
Wahyudi. 2000. Kimia Organik 3.
Jakarta : Depdikbud.